ESCLUSIVO: Perché la proteina Spike causa coaguli di sangue anormali, 200 sintomi

In questo documento in due parti, miriamo a fornire una panoramica coaguli di sangue anomali correlati a COVID-19, su come si formano, su come rilevarli precocemente e su come vengono trattati.
Speciale Epoch Times
Strani coaguli
Dalla metà del 2021, intutto il mondo sono stati segnalati coaguli di sangue insoliti e lunghi trovati nei vasi di pazienti COVID-19 e destinatari di vaccini.

“Noi come imbalsamatori stiamo vedendo alcuni strani coaguli dall’epidemia di COVID. Questi coaguli sono molto gommosi e molto lunghi in quanto escono dalle vene che usiamo durante la procedura di imbalsamazione. Sembrano davvero essere come lombrichi. Non l’ho mai visto nella mia carriera fino ad ora”, ha detto a The Epoch Times Larry Mills, un imbalsamatore autorizzato e direttore di pompe funebri nello Stato dell’Alabama.
Altri imbalsamatori hanno confermato risultati simili e hanno parlato a condizione di anonimato.
Richard Hirschman, direttore funebre dell’Alabama e imbalsamatore dal 2001, è stato uno dei primi a richiamare l’attenzione su questo fenomeno. Ha detto che prima del COVID forse dal 5 al 10% delle persone aveva questi coaguli. Ora più della metà dei corpi che vede li ha.
Un imbalsamatore, autorizzato dal 2001, ha detto in un’intervista: “Posso dirvi con certezza che i coaguli che Richard ha mostrato online sono un fenomeno a cui non ho assistito fino probabilmente alla metà dello scorso anno. Questo è praticamente tutto ciò che ho da dire al riguardo. Non ho alcuna conoscenza di ciò che sta causando i coaguli, ma apparentemente hanno iniziato a manifestarsi intorno alla metà del 2021”.
Da dove vengono questi strani coaguli fibrosi? Come si formano?
Una condizione con oltre 200 sintomi
I medici si sono resi conto, fin dai primi giorni della pandemia, che COVID-19 non è solo una malattia polmonare, ma anche una malattia endoteliale e vascolare.
I medici hanno riassunto un elenco diosservazioni cliniche insolitedi COVID-19, inclusi ma non limitati a pazienti gravemente ipossici (basso livello di ossigeno) nonostante la compliance polmonare relativamente normale all’esame, le complicanze trombotiche e i risultati autoptici coerenti di coaguli di sangue (trombi) nella microcircolazione del polmone.
Dopo un’infezione acuta da COVID-19, sono stati segnalati oltre 200 diversi sintomi persistentiper COVID lungo, che possonopersistere per circa 6-24 mesi.
Questo è forse il maggior numero di sintomi segnalati con una condizione medica finora.
I sintomi più frequenti includono affanno, affaticamento, nebbia del cervello, disfunzione cognitiva, dolori muscolari e dolori (mialgia), difficoltà a dormire e ansia o depressione.
Lanatura cronica e recidivante della COVID lungaè causata principalmente da disregolazione immunitaria, iperinfiammazione, stress ossidativo e disfunzione mitocondriale.
Ma come potrebbe essere, e perché? Gli indizi sono emersi dal 2020.
Coaguli di sangue che causano sintomi
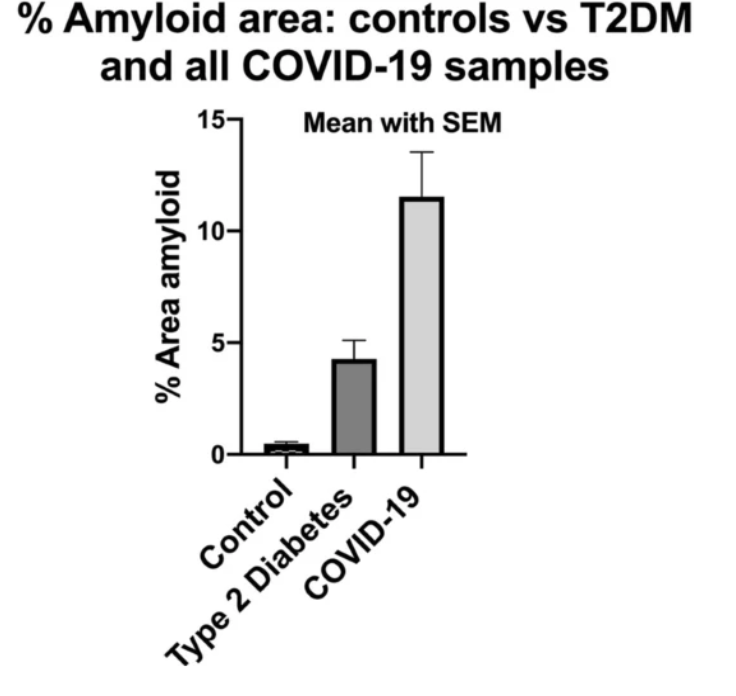
Nel novembre 2020, un rapporto con risultati diaumento dei microcoaguli nei pazienti COVID-19rispetto ai pazienti sani o diabetici potrebbe ragionevolmente spiegare la mancanza di respiro, l’affaticamento e la sindrome del malessere post-sforzo.
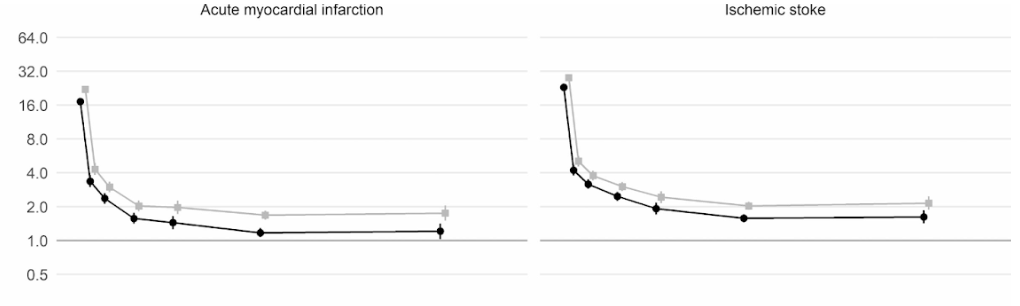
Inoltre, uno studio di coorte su larga scala del Regno Unito basato su 48 milioni di adulti in Inghilterra e Galles ha rilevato che nella prima settimana dopo una diagnosi di COVID-19, il rischio di un coagulo di sangue arterioso era quasi 22 volte superiore rispetto a qualcuno senza COVID-19 e 33 volte superiore per una condizione di coagulo venoso.
Un coagulo di arteria è il tipo che potrebbe causare un attacco di cuore o ictus ischemico bloccando il flusso di sangue al cuore o al cervello.
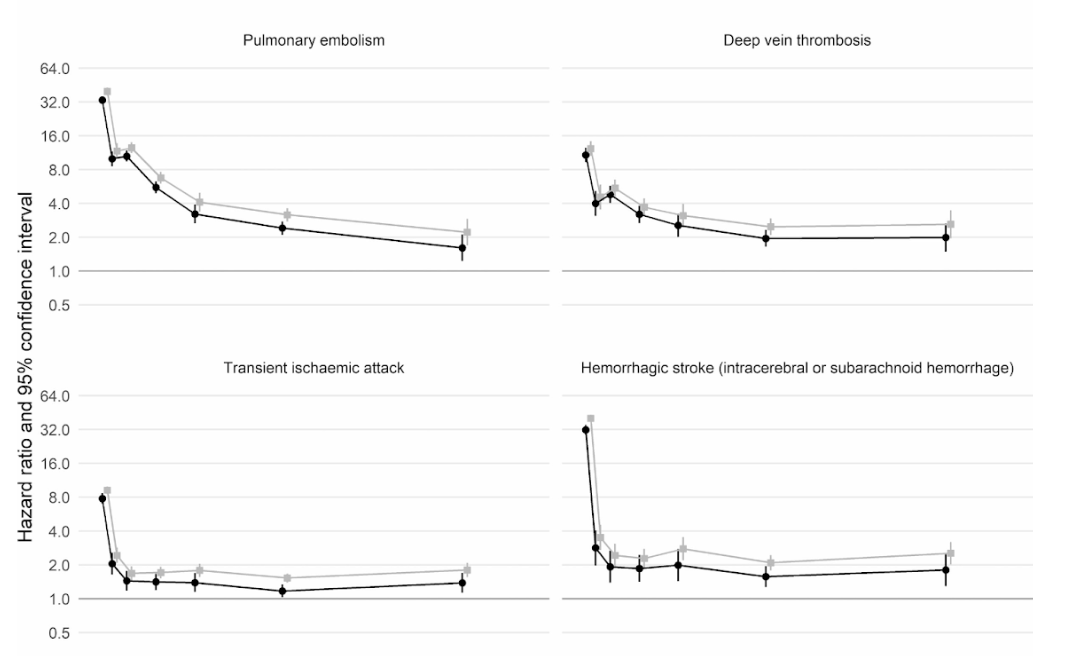
Ciò ha portato a circa 10.500 casi aggiuntivi di problemi legati al coagulo, cioè circa 7.200 ulteriori infarti o ictus e3.500 casi aggiuntivi di embolia polmonare, trombosi venosa profonda o altri problemi venosi.
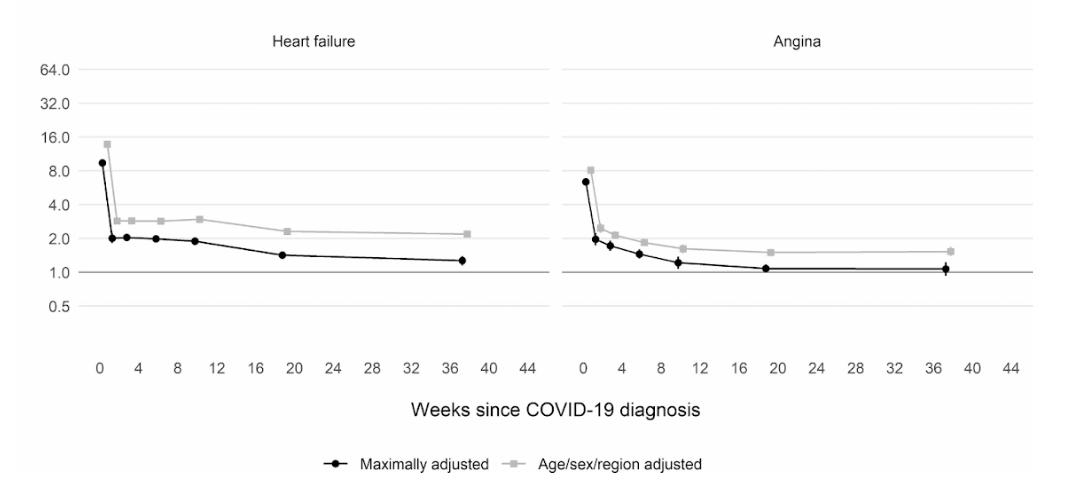
Anche se tale rischio scende bruscamente a meno di quattro volte superiore rispetto a qualcuno senza COVID nella seconda settimana, rimane elevato (2x) anche fino a 49 settimane dopo la diagnosi iniziale. Questo è particolarmente vero per quanto riguarda il rischio di trombosi venosa profonda. Questi sono coaguli che si formano in grandi vene.
Spike Protein: il primo domino rovesciato
Il sangue è un liquido che circola sotto pressione attraverso i vasi sanguigni in tutto il nostro corpo, come l’acqua che scorre attraverso la casa che poi usi per fare la doccia, lavare i piatti e così via.
A seguito di una lesione vascolare, qualsiasi sangue che “fuoriesce” deve essere rapidamente convertito in un gel (un “coagulo”) per riempire il foro e ridurre al minimo ulteriori perdite di sangue.
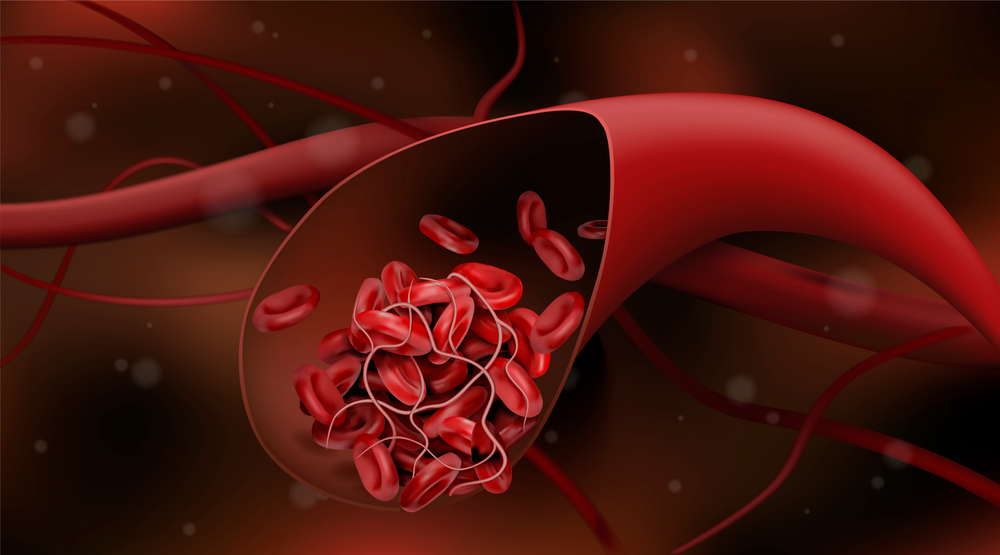
Normalmente, laporzione plasmatica del sangue contiene una raccolta di proteine solubiliche agiscono insieme inuna serie di eventi di attivazione enzimaticache provocano la formazione di un coagulo di fibrina. Questo processo è protettivo, in quanto previene un’eccessiva perdita di sangue a seguito di lesioni.
Sfortunatamente, il meccanismo di coagulazione del sangue può anche portare a coaguli di sangue indesiderati all’interno dei vasi sanguigni (trombosi patologica), ad esempio infarto o ictus, entrambi i quali sono una delle principali cause di disabilità e morte nel mondo.
Il modo in cui COVID-19 causacoaguli di sangue anomali ha stimolato molte discussionidall’inizio del 2020.
Sembra che la proteina spike unica del virus inneschi la cascata attraverso molti percorsi “non tradizionali”.
L’invasione diretta della proteina spike delle cellule dell’epitelio è il primo domino rovesciato.
I successivi effetti a cascata causano infine la coagulazione del sangue.
La proteina spike danneggia le cellule dell’epitelio
SARS-CoV-2 entra nelle nostre cellule attraverso un recettore proteico chiamato enzima di conversione dell’angiotensina 2 (ACE2).
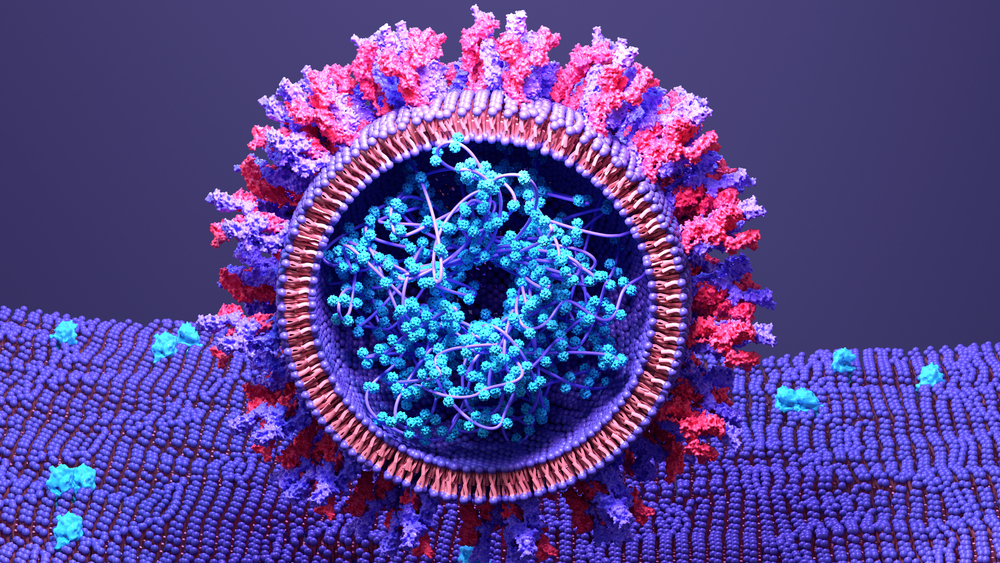
Le cellule endoteliali (ECs), esprimono un’abbondanza di ACE2. Le EC risiedono sulla superficie interna di ogni vaso sanguigno in tutto il nostro corpo, rendendole un bersaglio diretto dell’infezione virale.
Gli studi hanno dimostrato che la proteina spike stessapuò danneggiarela struttura e la funzione delle CE, tra cui compromettere i mitocondri e sottoregolare la molecola protettiva ACE2 sulle CE.
I ricercatori hanno osservato che entrambe le parti S1 e S2 della proteina spike possono indurre le EC umane ad esprimereun picco di citochine pro-infiammatorie (IL6, IL1B, TNF-alfa e chemochine CXCL1 e CXCL2).
Successivamente, il rilascio di citochine avvia la molecola simile a un interruttore (E-selectina) sulla membrana cellulare endoteliale, consentendo loro di attaccarsi con le cellule immunitarie, avviando così i successivi processi patologici.
Ulteriori studi sulla proteina spike hanno dimostrato che attiva l’infiammazione EC dipendente dalle vie disegnalazione dell’integrina ⍺5β1 e NF-κB edalla successiva espressione delle molecole di adesione dei leucociti.
Le citochine sono piccole proteine secrete dalle cellule (principalmente cellule T e macrofagi). Hanno molti nomi specifici e fungono da comunicatore tra le cellule (segnalazione cellulare) per ulteriori azioni. Le citochine sono i “postini” del corpo che si collegano e comunicano tra le cellule.
La proteina spike può indurre unarottura delle proteine di collegamento tra le cellule endoteliali dei vasi sanguigni, che interrompe l’integrità e la funzione dei nostri vasi sanguigni.
Anche le EC cerebrali esprimono fortemente ACE2. La proteina spikeha effetti tossici simili sulle EC cerebrali, inducendo sintomi neurologici (nebbia cerebrale, declino cognitivo).
Le proteine spike innescano la cascata di coagulazione
Molte altre cellule, tra cui le cellule epiteliali polmonari, gli enterociti che rivestono l’intestino tenue e i periciti cardiaci, esprimono tutti ACE2.
Le proteine spike non solo attivano le cellule epiteliali (EC) e promuovono l’infiammazione localizzata. Promuovono anche l’infiammazione sistemica poiché ACE2 è quasi ovunque all’interno dei nostri principali organi e tessuti.
Di conseguenza, vengono espressi più geni pro-infiammatori. Sempre più cellule immunitarie vengono attratte e inviate ai tessuti feriti o infetti (vasi nei polmoni, nel cuore, nell’intestino, ecc.).
Un certo numero di eventi successivi contribuiscono collettivamente alla cascata di coagulazione:
- Infiammazione mediata dal complemento degli epiteli (endotelielite): le proteine spike che si agganciano alle EC ACE2 attivano la via del complemento e la cascata della coagulazione, causando endotelielite sistemica (danno polmonare) e stato procoagulante (tendenza a sviluppare coaguli di sangue).
- Quando il complemento distrugge l’endotelio, vengono rilasciati il fattore procoagulante di von Willebrand (vWF) e FVIII. Un aumento significativo di vWF può formare multimeri che promuovono la crescita dei trombi. La vWF è secreta principalmente dalle cellule endoteliali e dai granuli A delle piastrine (derivati dai megacariociti). Questo è paragonabile alla corda nelle “perline e spago” di una collana in cui le perle rappresentano piastrine.
- Tempesta piastrinica: Le piastrine sono un piccolo frammento dei megacariociti. Le anafilotossine del complemento C3a e C5a attivano le piastrine e aumentano la produzione di fattore tissutale promuovendo ulteriormente uno stato di formazione della coagulazione.
I recettori ACE2 sono presenti sulle piastrine e questo può contribuire alla massiccia aggregazione piastrinica, che è una caratteristica della grave infezione da COVID-19. - L’attivazione dei neutrofili porta alla formazione di trappole extracellulari dei neutrofili (NET), un processo a volte indicato comeNETosis, che contribuisce alla trombosi.
- Il danno EC è aggravato dall’attivazione del recettore toll-like (TLR) mediante il riconoscimento dell’RNA virale, con conseguenteaumento della produzione di specie ossidative reattive (ROS). L’aumento del ROS aumenta ulteriormente l’espressione di vWF.
- La proteina spike può indurre l’espressione e la secrezione diuna serie di proteine della coagulazione che si riversano nel processo di coagulazione, tra cui il fattore (F)-V, la trombina e il fibrinogeno per promuovere il processo di coagulazione.
La proteina spike disregola il RAAS, peggiorando lo stato di coagulazione
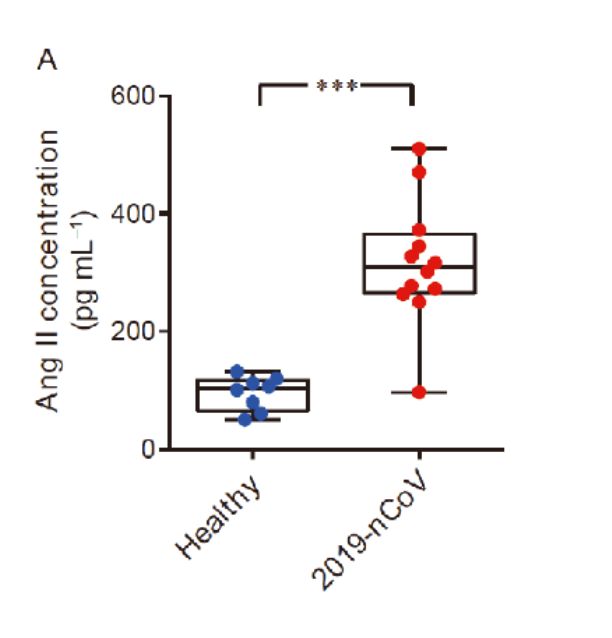
A causa della proteina spike che interagisce direttamente con l’espressione di ACE2, i pazienti COVID-19 hanno mostrato unlivello elevato di angiotensina II siericache indica una disregolazione del sistema RAA (sistema renina-angiotensina aldosterone, o RAAS).
Tradizionalmente, la gente pensa che l’angiotensina II sia un neuroormone che stimola la costrizione delle cellule muscolari lisce vascolari ed è responsabile dell’equilibrio salino e idrico.
Tuttavia, ci sono stati numerosi studi a sostegno dell’idea chel’angiotensina II sia in grado di avviare e sovraregolare le risposte infiammatorie, peggiorando lo stato di coagulazione.
In una risposta immunitaria regolata e autolimitata, questi meccanismi aiutano a calmare la lesione locale, con successiva guarigione e ritorno a uno stato EC a riposo.
Tuttavia, per i pazienti COVID-19 predisposti o le persone vaccinate, i fattori che rafforzano la formazione di coaguli sono molto più pesanti dei meccanismi di guarigione, che portano tutti a unacascata trombotica crescente.
Ecco un breve riassunto della prima scena della storia del coagulo: interruzione endoteliale indotta da spike, massicce quantità di vWF rilasciate, una successiva tempesta piastrinica, upregulation indotta dall’ipossia e attivazione del vWF, rete fibrosa da trappole extracellulari di neutrofili (NET), nonché aumento del livello di angiotensina II, che si sommano per avviare la trombogenesi.
Ecco come nasce il meccanismo di coagulazione. Inoltre, l’imminente seconda scena assume un’altra parte fondamentale nell’intera storia.
Un vaccino COVID istruisce le cellule a produrre grandi quantità di proteine spike. I normali processi biochimici e fisiologici vengono “dirottati” per produrre una quantità anormale di queste proteine spike.
Queste quantità anormali di proteina spike hanno effetti diretti più sorprendenti sui coaguli.
Le proteine spike interrompono direttamente il meccanismo di dissoluzione del coagulo
In una persona sana normale, il corpo, in presenza di un coagulo di sangue, lo abbatterà con un processo di fibrinolisi. Questo è un meccanismo naturale di guarigione e bilanciamento per prevenire l’abbondanza di coaguli di sangue.
Durante questo processo, l’attivatore tissutale del plasminogeno (TPA, proveniente dall’endotelio) aiuta il plasminogeno a trasformarsi in plasmina e quindi a generare d-dimero (un piccolo frammento proteico rimasto quando un coagulo di sangue si dissolve).
È stato scoperto che il fibrinogeno nel sangue può coagularsi in una forma anormale di “amiloide” di fibrina che (come altri amiloidi e prioni ricchi di β) è relativamente resistente alla proteolisi (fibrinolisi).
Ciò si manifesta fortemente nel plasma povero di piastrine (PPP) di individui con COVID lungo. Gli estesi microcoaguli amiloidi di fibrina possono persistere.
In uno studio eccezionale di Grobbelaar pubblicato su Bioscience Reports nell’agosto 2021, il biomarcatore S1 (o la parte intrusa della proteina spike) da solo puòindurre resistenza alla fibrina alla fibrinolisi, portando alla formazione di microcoaguli incontrastati.
Quando la proteina spike S1 è stata aggiunta a PPP sani, ha provocato cambiamenti strutturali a β e γ fibrina (ogen), complemento 3 e protrombina. Queste proteine erano sostanzialmente resistenti alla tripsinizzazione in presenza della proteina spike S1.
Quindi, i risultati suggeriscono che la presenza di proteina spike in circolazione può contribuire allo stato di ipercoagulazione e può causare una sostanziale compromissione del processo di dissoluzione del coagulo.
Tale compromissione litica può causare i microcoaguli di grandi dimensioni persistenti che le persone hanno segnalato e che sono stati trovati in campioni di plasma di pazienti COVID-19.
Questi microcoaguli bloccano i capillari, e quindi limitano il passaggio dei globuli rossi, e quindi lo scambio di ossigeno, che può effettivamente sostenere la maggior parte di questi sintomi.
Le proteine spike formano una sostanza amiloide-simile
Inoltre, con sorpresa di tutti, le proteine spike sono identificate perpresentare sette sequenze amiloidogeniche e sono in grado di formare sostanze amiloidi.
In altre parole, queste proteine spike sono simili a quelle sostanze simili all’amiloide-beta o alla tau o all’alfa-sinucleina che possono causare perdita neuronale nei pazienti con malattia di Alzheimer o Parkinson.
La loro struttura rende facile formare strutture legate simili a corde più strette con torsione longitudinale e legame incrociato, formando una struttura fibrosa visibile al microscopio.
I ricercatori hanno scoperto che i campioni di plasma dipazienti COVID lunghicontengono ancora grandi depositi anomali (amiloide) (microcoaguli), che sono resistenti alla fibrinolisi (rispetto al plasma dei controlli e al diabete), anche dopo la tripsinizzazione (dissociazione cellulare dopo che un enzima scompone le proteine).
Dopo una seconda tripsinizzazione, i depositi persistenti di pellet (microcoaguli) sono stati solubilizzati. Varie molecole infiammatorie sono aumentate sostanzialmente sia nel surnatante che intrappolate nei depositi di pellet solubilizzati di COVID-19, rispetto a quello dei campioni di controllo.
Di particolare interesse è stato un sostanziale aumento della α(2)-antiplasmina (α2AP), varie catene di fibrinogeno, nonché dell’amiloide sierica A (SAA) che sono state intrappolate nei depositi di pellet solubilizzati resistenti ai fibrinolitici.
Una significativa formazione anomala di microcoaguli amiloidi resistenti alla fibrinolisi, l’aumento di α2AP e l’aumento delle molecole infiammatorie in fase acuta possono quindi contribuire in modo centrale sia all’infezione da COVID-19 che alla sindrome correlata al vaccino COVID.
La proteina spike inibisce un altro meccanismo anticoagulo
La proteina spike è solo una sorpresa dopo l’altra.
È stato riportato che laproteina spike può inibire in modo competitivo i legami dell’antitrombina e del cofattore II dell’eparina all’eparina, causando un aumento anormale dell’attività della trombina (coagulazione).
Le proteine spike di SARS-CoV-2 a una concentrazione simile (~10 μg/ml) della carica virale nei pazienti critici possono causare direttamente coagulazione del sangue e trombosi nel modello zebrafish.
Per riassumere, questi effetti negativi inaspettati della proteina spike sul processo di dissoluzione dei coaguli di sangue, oltre alla sua natura amiloide, possono essere tutti i fattori chiave che contribuiscono ai coaguli fibrosi anormali e lunghi osservati in condizioni correlate al COVID.
Spike Protein è la pistola fumante
Esistono prove cliniche che laproteina spike SARS-CoV-2 è stata rilevata in coaguli recuperati da pazienti COVID-19con ictus ischemico acuto e infarto del miocardio.
Una recente ricerca condotta da cardiologi dell’Università del Colorado fa luce sul ruolo cruciale della proteina spike nella patologia del COVID e delle lesioni correlate al vaccino COVID.
Hanno analizzato sette pazienti COVID-19 e sei pazienti vaccinati con mRNA con lesioni miocardiche e hanno trovatoalterazioni quasi identiche nei modelli di profilazione genica che li predisporrebbero allo stato di coagulazione, all’infiammazione e alla disfunzione miocardica.
In altre parole, indipendentemente dal fatto che la miocardite sia stata causata dal virus o dal vaccino, l’espressione dei geni responsabili dello stato protrombotico in risposta alla proteina spike, all’infiammazione e alla disfunzione miocardica, ha mostrato cambiamenti simili.
Sulla base dell’analisi genica, COVID-19 e lesioni da vaccino post-mRNA hanno un meccanismo molecolare comune.
Il modello dei geni alterati include la down-regulation in ACE2, ACE2/ACE, AGTR1 e ITGA5 e l’up-regulation in ACE e F3 (fattore tissutale).
Ciò che è più allarmante e non riportato prima è che la trombosi microvascolare è stata trovata in pazienti post-vaccinati, indicando che la proteina spike stessa è in grado di innescare coaguli di sangue in pazienti sensibili.
Punta dell’iceberg
Sulla base della relazione causale tra i vaccini ChAdOx1-S (il vaccino COVID adenovirus di AstraZeneca) e la trombosi con sindrome trombocitopenica, leinformazioni sul prodotto per ChAdOx1-S sono state aggiornate perincludere la trombosi con sindrome trombocitopenia come effetto collaterale molto raro.
Questo è stato chiamatotrombocitopenia trombotica immunitaria indotta dal vaccino (VITT), a causa del fatto che in quasi tutti i pazienti in questi rapporti, alti livelli di anticorpi contro ilfattore piastrinico 4 (PF4)-complessi polianionici sono stati identificati nel loro corpo.
Questi coaguli di sangue insoliti in combinazione con trombocitopenia sono stati riportati prevalentemente in donne di età inferiore ai 60 anni. Di conseguenza, diversi paesi europei hanno limitato l’uso dei vaccini adenovirus nelle fasce di età più giovani.
Questo rischio è stato recentemente analizzato sistematicamente in uno studio di coorte della rete internazionale di cinque paesi europei e degli Stati Uniti, confermando unaumento del 30%del rischio di trombocitopenia dopo una prima dose del vaccino ChAdOx1-S, nonché una tendenza verso un aumento del rischio di trombosi venosa con sindrome trombocitopenia dopo Ad26.COV2.S (il vaccino COVID Janssen) rispetto a BNT162b2 (il vaccino COVID di Pfizer-BioNTech).
Tuttavia questa potrebbe essere solo la punta dell’iceberg. Ci sono molti altri eventi che potrebbero essere attribuiti ai problemi di coagulazione tra cui morte improvvisa, eventi cardiovascolari, morte cardiaca, ictus, disabilità, eventi trombotici, ecc.
I vasi sanguigni sono in tutti i nostri organi. I problemi dei vasi potrebbero spiegare una vasta gamma di sintomi dalla disfunzione al lieve declino del nostro cervello, cuore, polmone e estremità.
a cura del Dr. Yuhong Dong, un medico che ha anche conseguito un dottorato in malattie infettive in Cina, è il direttore scientifico e co-fondatore di una società biotecnologica svizzera ed ex esperto medico scientifico senior per lo sviluppo di farmaci antivirali presso Novartis Pharma in Svizzera.
Con la segnalazione aggiuntiva di Enrico Trigoso.
